Понятие спирта
С точки зрения химии, спирты – большая группа сложных органических соединений, в составе которых обязательно присутствует одна или несколько гидроксильных групп (-ОН). Причем каждая из них связана с атомом углерода. В зависимости от количества гидроксильных групп определяется атомность спирта (одно-, двух- или трехатомный).
С физической точки зрения, спирт – летучая, легко воспламеняющаяся, бесцветная жидкость с характерным запахом и вкусом. Ее получают путем дистилляции перебродивших сырых веществ, имеющих в составе крахмал или сахар. Сырьем для получения спирта могут служить:
- фрукты (виноград, яблоки, сливы);
- зерно (пшеница, рожь, ячмень, кукуруза);
- овощи (картофель, свекла).
Фрукты и овощи
Разнообразные спирты широко распространены в природе (чаще всего в составе эфирных масел), выполняют важные функции внутри живых организмов, активно используются в различных областях промышленности.
Применение этанола в качестве автомобильного топлива
В разных странах действуют разные государственные программы применения этанола на транспорте:
| Страна | Требования |
|---|---|
| США | производит ежегодно 28 млрд литров этанола к 2012 году, 85%-я смесь этанол/бензин (E85) |
| Евросоюз | 2 % в 2005, 5,75 % биотоплив к 2010 году (этанол + биодизель) |
| Китай | производить ежегодно 3 млн тонн к 2010 году |
| Таиланд | В Бангкоке 10%-я смесь, 5%-я смесь по всей стране с 2007 года |
В США «Энергетический билль», подписанный президентом Бушем в августе 2005 года, предусматривает производство к 2012 году ежегодно 30 миллиардов литров этанола из зерна и 3,8 миллиардов литров из целлюлозы (стебли кукурузы, рисовая солома, отходы лесной промышленности).
Этанол хорошо смешивается с водой, в отличие от бензина. Проблема расслаивания смеси бензина и этанола на данный момент не решена.
Автомобильный парк, работающий на этаноле
Смесь этанола с бензином обозначается буквой Е. Цифрой у буквы Е обозначается процентное содержание этанола. Е85 — означает смесь из 85 % этанола и 15 % бензина.
Смеси до 20 % содержания этанола могут применяться на любом автомобиле. Однако некоторые производители автомобилей ограничивают гарантию при использовании смеси с содержанием более 10 % этанола. Смеси, содержащие более 20 % этанола, во многих случаях требуют внесения изменения в систему зажигания автомобиля.
Автопроизводители выпускают автомобили, способные работать и на бензине, и на Е85. Такие автомобили называются «Flex-Fuel». В Бразилии такие автомобили называют «гибридными». В русском языке названия нет. Большинство современных автомобилей либо изначально поддерживают использование такого топлива, либо опционально, по соответствующему запросу.
В 2005 году в США более 5 млн автомобилей имели Flex-Fuel двигатели. В конце 2006 г. в США эксплуатировалось 6 млн автомобилей с Flex-Fuel двигателями. Общий автопарк составляет 230 млн автомобилей.
1200 заправочных станций продают Е85 (май 2007). Всего в США автомобильное топливо продают около 170 000 заправочных станций.
В Бразилии около 29 000 заправочных станций продают этанол.
Экономичность
Себестоимость бразильского этанола (около 0,19 долларов США за литр в 2006 г.) делает его использование экономически выгодным.
Экологические аспекты
Биоэтанол как топливо нейтрален в качестве источника парниковых газов. Он обладает нулевым балансом диоксида углерода, поскольку при его производстве путём брожения и последующем сгорании выделяется столько же CO2, сколько до этого было взято из атмосферы использованными для его производства растениями.
В 2006 году применение этанола в США позволило сократить выбросы около 8 млн тонн парниковых газов (в СО2 эквиваленте), что примерно равно годовым выхлопам 1,21 млн автомобилей.
Использование метилового спирта
Несмотря на свое ядовитое воздействие на организм человека, метиловый спирт крайне полезен в промышленном применении. Сферой распространения жидкости стали:
химическая отрасль – производство пластмассы, антифризов и растворителей;
топливная отрасль – используют в качестве топлива для спортивных автомобилей;
пищевая промышленность – изготавливают метиловый концентрат в качестве вкусовой добавки к пищевым продуктам. Он прекрасно сочетается с любыми продуктами, в том числе фруктами, овощами, мясом, рыбой. Метиловый и этиловый спирты применяются в производстве кондитерских изделий, при изготовлении различных лекарств и средств косметики.
газовая промышленность – применяют в борьбе с образованием гидратов.
Разнообразное использование метанола возможно из-за химических особенностей жидкости:
при смешивании с водой происходит химическая реакция с выделением тепла;
низкая температура закипания – 64, 5 0С;
легковоспламеняющаяся жидкость с голубовато-зеленоватым оттенком.
Для производства метилового и этилового спиртов используется метанол. Процесс получения этиловых спиртов ведут из метанола в присутствии щелочных агентов – щелочи или аммиака. При окислении метанола образуется формальдегид .
Именно химические свойства метанола легли в основу методик распознавания вида спиртов по назначению.
Способы получения
1. Гидролиз галогеналканов. Вы уже знаете, что образование галогеналканов при взаимодействии спиртов с галогено-водородами — обратимая реакция. Поэтому понятно, что спирты могут быть получены при гидролизе галогеналканов — реакции этих соединений с водой.
Многоатомные спирты можно получить при гидролизе галогеналканов, содержащих более одного атома галогена в молекуле.
2. Гидратация алкенов — присоединение воды по тг-связи молекулы алкена — уже знакома вам. Гидратация пропена приводит в соответствии с правилом Марковникова к образованию вторичного спирта — пропанола-2
ОН lСН2=СН—СН3 + Н20 -> СН3—СН—СН3 пропен пропанол-2
3. Гидрирование альдегидов и кетонов. Вы уже знаете, что окисление спиртов в мягких условиях приводит к образованию альдегидов или кетонов. Очевидно, что спирты могут быть получены при гидрировании (восстановлении водородом, присоединении водорода) альдегидов и кетонов.
4. Окисление алкенов. Гликоли, как уже отмечалось, могут быть получены при окислении алкенов водным раствором перманганата калия. Например, этиленгликоль (этандиол-1,2) образуется при окислении этилена (этена).
5. Специфические способы получения спиртов. Некоторые спирты получают характерными только для них способами. Так, метанол в промышленности получают при взаимодействии водорода с оксидом углерода(II) (угарным газом) при повышенном давлении и высокой температуре на поверхности катализатора (оксида цинка).
Необходимую для этой реакции смесь угарного газа и водорода, называемую также (подумайте почему!) «синтез-газ», получают при пропускании паров воды над раскаленным углем.
6. Брожение глюкозы. Этот способ получения этилового (винного) спирта известен человеку с древнейших времен.
Рассмотрим реакцию получения спиртов из галогеналканов — реакцию гидролиза галогенпроизводных углеводородов. Ее обычно проводят в щелочной среде. Выделяющаяся бромоводородная кислота нейтрализуется, и реакция протекает практически до конца.
Эта реакция, как и многие другие, протекает по механизму нуклеофильного замещения.
Это реакции, основной стадией которых является замещение, протекающее под воздействием нуклеофильной частицы.
Напомним, что нуклеофильной частицей является молекула или ион, имеющая неподеленную электронную пару и способная притягиваться к «положительному заряду» — участкам молекулы с пониженной электронной плотностью.
Наиболее распространенными нуклеофильными частицами являются молекулы аммиака, воды, спирта или анионы (гидроксил, галогенид, алкоксид-ион).
Частицу (атом или группу атомов), замещаемую в результате реакции на нуклеофил, называют уходящей группой.
Замещение гидроксильной группы спирта на галогенид-ион также протекает по механизму нуклеофильного замещения:
СН3СН2ОН + НВг —> СН3СН2Вг + Н20
Интересно, что эта реакция начинается с присоединения катиона водорода к атому кислорода, содержащегося в гидроксильной группе:
СН3СН2—ОН + Н+ —> СН3СН2— ОН
Под действием присоединившегося положительно заряженного иона связь С—О еще больше смещается в сторону кислорода, эффективный положительный заряд на атоме углерода увеличивается.
Это приводит к тому, что нуклеофильное замещение на галогенид-ион происходит гораздо легче, а отщепляется под действием нуклеофила молекула воды.
СН3СН2—ОН+ + Вг —> СН3СН2Вг + Н2O
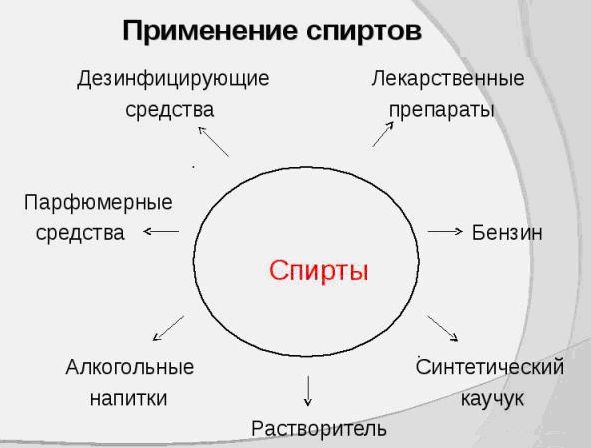
Применение спиртов
Так как спирты имеют разнообразные свойства, то и область из применения довольно таки обширна. Давайте с вами попробуем разобраться, где же применяются спирты.
Спирты в пищевой промышленности
Такой спирт, как этанол является основой всех алкогольных напитков. А получают его из сырья, которое содержит сахар и крахмал. Таким сырьем может быть сахарная свекла, картофель, виноград, а также разные злаковые культуры. Благодаря современным технологиям при производстве спирта происходит его очистка от сивушных масел.
В натуральном уксусе также присутствует сырье, полученное на основе этанола. Этот продукт получается благодаря окислению уксуснокислым бактериям и аэрированию.
Но в пищевой промышленности используют не только этанол, но и глицерин. Эта пищевая добавка способствует соединению несмешиваемых жидкостей. Глицерин, который входит в состав ликеров, способен придавать им вязкость и сладкий вкус.
Также, глицерин применяют при изготовлении хлебобулочных, макаронных и кондитерских изделиях.
Медицина
В медицине этанол просто незаменим. В этой отрасли он широко применяется в качестве антисептика, так как обладает свойствами, которые способны уничтожать микробы, задерживать болезненные изменения в крови и не допускают разложения в открытых ранах.
Этанолом пользуются медицинские работники перед проведением различных процедур. Этот спирт обладает свойствами обеззараживания и просушивания. При проведении искусственной вентиляции легких, этанол выступает в роли пеногасителя. А также этанол может быть одним из компонентов при анестезии.
При простуде этанол можно использовать, как согревающий компресс, а при охлаждении, как средство для растирания, так как его вещества способствуют восстановлению организма при жаре и ознобе.
В случае отравления этиленгликолем или метанолом, применение этанола способствует уменьшению концентрация токсичных веществ и выступает в роли противоядия.
Также огромную роль спирты оказывают фармакологии, так как они используются для приготовления целебных настоек и всевозможных экстрактов.
Спирты в косметике и парфюмерии
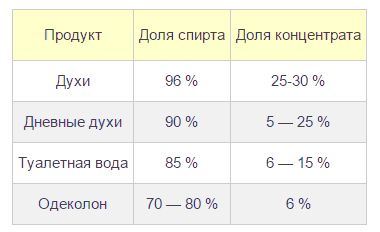
В парфюмерии без спиртов также никак не обойтись, так как основой практически всех парфюмерных продуктов является вода, спирт и парфюмерный концентрат. Этанол в этом случае выступает в роли растворителя душистых веществ. А вот 2-фенилэтанол обладает цветочным запахом и в парфюмерии может заменить натуральное розовое масло. Его применяют при изготовлении лосьонов, кремов и т.д.
Глицерин также является основой базы для многих косметических средств, так как имеет способность притягивать влагу и активно увлажнять кожу. А присутствие этанола в шампунях и кондиционерах способствует увлажнению кожных покровов и облегчает расчесывание волос после мытья головы.
Топливо

Ну а такие спиртосодержащие вещества, как метанол, этанол и бутанол-1 широко используются в качестве топлива.
Благодаря переработке такого растительного сырья, как сахарный тросник и кукуруза,
удалось получить биоэтанол, который является экологически чистым биотопливом.
В последнее время производство биоэтанола стало популярным в мире. С его помощью появилась перспектива в возобновлении топливных ресурсов.
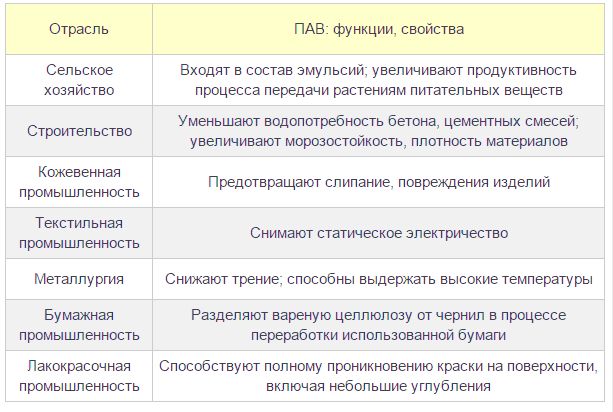
Растворители, поверхностно-активные вещества
Кроме уже перечисленных сфер применения спиртов, можно отметить и то, что они
еще являются и хорошими растворителями. Наибольшей популярностью в этой области пользуются изопропанол, этанол, метанол. Они также используются при производстве битовой химии. Без них не возможен полноценный уход за автомобилем, одеждой, домашней утварью и т.д.
Использование спиртов в разных сферах нашей деятельности положительно влияет на нашу экономику и приносит комфорт в нашу жизнь.
Безводный спирт
Безводные спирты ( 5 — 50 мг) растворяют в 5 мл бензола, добавляют 50 мг 3 5-динитробензоилхлорида и 0 3 мл пиридина и в течение часа кипятят в колбе с обратным холодильником.
Безводный спирт, впервые полученный Ловицем ( ст. 7 в разд. IV), был введен им в аналитическую практику. В данной статье описан замечательный метод, разработанный Ловицем для разделения хлоридов бария и стронция с помощью безводного спирта.
Безводные спирты при обычных температурах хорошо смешиваются с бензином в любых соотношениях, однако незначительные примеси воды вызывают расслоение смеси. Для предупреждения расслаивания спирто-бензиновых топливных композиций ( СБТК) в их состав вводят специальные стабилизаторы — сорастворители. В настоящее время одним из основных факторов, сдерживающих широкое применение данных композиций, является дефицит эффективных сорастворителей.
Смесь безводного спирта и бензола разделяется на второй колонне ( низкого давления), причем безводный спирт вытекает снизу, а оензол в виде паров идет в дефлегматор и холодильник и далее в колонну высокого давления. Выходящая из холодильника смесь бензола, воды и спирта разделяется на два слоя, из которых верхний ( оензольный) направляется обратно в колонну высокого давления, а нижний ( водно-спиртовой) разделяется в дополнительной колонне. Спирт из этой колонны направляется обратно в колонну высокого давления, а вода, вытекающая из нижней части колонны, покидает установку. Таким образом в этой установке, так же как и в предыдущей, бензол и часть спирта все время циркулируют внутри системы колонн.
Из безводного спирта, поступающего в куб, 92 % уходит в ректификат I сорта.
Количество безводного спирта, отходящего с головными продуктами из эпюрационной колонны, принимаем в среднем равным 3 % от всего введенного в аппарат алкоголя. С сивушным маслом уходит — 0 4 % алкоголя по массе, введенной в аппарат.
Количество безводного спирта, содержащееся в водно-спиртовом растворе, отнесенное к его нормальной температуре ( 20 С), выражается произведением от умножения объема раствора на множитель объемного содержания в нем безводного спирта при фактических температуре и крепости данного раствора.
Количество безводного спирта находится при помощи таблиц для определения содержания этилового спирта в водно-спиртовых растворах при 20 С, утвержденных Комитетом стандартов, мер и измерительных приборов при Совете Министров СССР.
С безводным спиртом эфир смешивается во всех соотношениях. Эфир весьма летуч и легко воспламеняется. Распространяясь в воздухе, пары его образуют гремучке смеси, почему он является веществом чрезвычайно огнеопасным.
В безводных спиртах в присутствии НС1 цирконий растворяется легче, чем в воде. Предполагается, что защитные свойства возникающих в данных условиях хлоридных пассивирующих слоев хуже защитных свойств окис-ных слоев, образующихся в водных растворах.
В безводном спирте могут получаться из оксиальдегидов простые эфиры изомерных кетоспиртов как особое направление реакции.
В безводном спирте концентрация RJOH2 приравнена концентрации № или, в случае минеральной кислоты — концентрации последней.
В безводном спирте концентрация R2OHa приравнена концентрации Н или, в случае минерально кислоты-концентрации последней.
В безводных спиртах в присутствии НС1 цирконий растворяется легче, чем в воде. Предполагается, что защитные свойства возникающих в данных условиях хлоридных пассивирующих слоев хуже защитных свойств окис-ных слоев, образующихся в водных растворах.
Можно применять безводный спирт, полученный перегонкой азео-тропной смеси с бензолом.
Распространение в природе
В природе спирты встречаются в свободным виде. Вещества также являются компонентами сложных эфиров. Естественный процесс брожения содержащих углеводы продуктов создает этанол, а также бутанол-1, изопропанол. Спирты в хлебопекарной промышленности, пивоварении, виноделии связано с использованием процесса брожения в этих отраслях. Большая часть феромонов насекомых представлена спиртами.

Спиртовые производные углеводов в природе:
сорбит — содержится в ягодах рябины, вишни, имеет сладкий вкус.
Многие растительные душистые вещества — это терпеновые спирты:
- фенхол — компонент плодов фенхеля, смол хвойных деревьев
- борнеол — составной элемент древесины борнеокамфорного дерева
- ментол — компонент состава герани и мяты
Желчь человека, животных содержит желчные многоатомные спирты:
- миксинол
- химерол
- буфол
- холестанпентол
Питьевой этанол
Данный вид изготавливают из крахмалистого сырья, которое является основой для производства алкогольных напитков. Его крепость составляет 95%. Показатели качества определяют на основании физико-химических анализов. Согласно требованиям государственного стандарта, эта разновидность спирта не должна содержать более 4 мг/дм3 альдегидов и сивушных масел.
Качество продукта, поставляемого в розничную торговую сеть, проверяют органолептическим и физико-химическим методами. В соответствии с ГОСТом Р 51698-2000 Спирт этиловый питьевой 95%-ный в эту разновидность включены такие компоненты как сахар и вода. Для изготовления данного вида продукции используют пшеницу, ячмень, рис и кукурузу. При использовании пшеницы, ячменя, риса и кукурузы содержание сахара должно быть не менее 0,65%.
Виды спирта для производства водки

Классификация спиртов, в том числе и для водки, включает в себя шесть основных видов:
- первого сорта;
- спирт высшей очистки;
- базис;
- экстра;
- люкс;
- альфа.
К основным сортам, используемым для производства водки, относятся все перечисленные, за исключением спирта первого сорта. Он не используется для производства алкогольной продукции, а применяется исключительно в технических целях. Хотя это не уменьшает риска встретить так называемый «подпольный» алкоголь, сделанный на его основе. Употребление такой продукции опасно не только для здоровья, но и для жизни человека.
Разнообразие марок спирта для производства водки впечатляет. Это влечет за собой возникновение множества споров о том, какой из спиртов самый лучший для вкусовых качеств водки. Ответ кроется в характеристике каждого из сортов. Ведь все они отличаются степенью очистки. Качество спирта определяет концентрация сивушных масел во взятом объеме жидкости. Чем она ниже, тем качественнее спирт. Помимо этого, к основным характеристикам качества этилового ректификованного спирта, регламентированным государственным стандартом, относятся:
- Прозрачность – жидкость не должна иметь мутный оттенок или содержать какие-либо примеси, видные невооруженным взглядом. Такой продукт не отвечает минимальным требованиям и пригоден только в технических целях.
- Вкус и запах – по ГОСТу в спирте не должно улавливаться никаких привкусов и посторонних запахов (особенно сивушных).
По ГОСТу основные сорта спирта для водки обладают следующими качествами:
- Спирт высшего сорта. Изготавливается из зерна, картофеля, патоки, сахарной свеклы, взятых в любых пропорциях. Встретить алкогольную продукцию на основе только этого вида непросто – в основном он используется в качестве основы для наливок и настоек. Из-за минимальной фильтрации примесей получаемая из него водка относятся к низшему ценовому сегменту.
- Базис. Для его приготовления картофель и зерновые культуры также берутся в произвольных пропорциях, но процент содержания картофельного крахмала в получаемом сырье не должен превышать отметки 60%.
- Экстра. Имеет сходный с базисным состав, но характеризуется более тщательной очисткой, в результате чего снижается процент содержания метанола и вредных примесей. Сорта Экстра и Базис – основа для производства водки среднего качества.
- Люкс. Результат смеси картофеля и зерна, при котором содержание крахмала не должно превышать 35%. Подвергается нескольким этапам фильтрации. Спирт люкс применяется для производства водки премиум-класса.
- Альфа — самый дорогой и самый качественный сорт спирта. Для его изготовления применяются зерна ржи и пшеницы самого высокого качества. Спирт Альфа подвергается самой высокой степени очистки, что сводит возможное содержание метанола в нем к минимуму. На основе этого сорта производятся самые дорогие и качественные сорта водки, предназначенные чаще для экспорта.
Хотя водочное сырье не должно обладать какими-либо выраженными вкусовыми качествами, любой ценитель «беленькой» с уверенностью скажет, что каждая водка обладает своим вкусом. Это объясняется тем, что редкий продукт изготавливается на основе только одного вида этанола. Почти любая марка напитка представляет собой смесь нескольких спиртов разного класса.
Индивидуальные вкусовые качества и ароматы напитка обусловлены также содержанием в каждом из них различных добавок. Они призваны смягчать вкус водки и выделять ее на фоне внушительного числа аналогов. К таким вкусовым добавкам могут относиться:
- сахар;
- лимонная кислота;
- талая вода;
- экстракты ягод или фруктов;
- березовый сок;
- мед;
- красный перец;
- экстракты трав;
- кедровые орешки.
Разнообразие добавок не уступает разнообразию самой продукции. Главное, чтобы они не влияли на прозрачность готового напитка и не выпадали в осадок.
Диэтиловый эфир
Смешанные спирты: увлекательный мир комбинаций
В парфюмерии существует широкий спектр спиртов, используемых в процессе создания ароматов. Одним из наиболее интересных типов спиртов являются смешанные спирты. Они представляют собой комбинацию различных алкоголей, которые обладают своими особенностями и свойствами.
Смешанные спирты предлагают парфюмерам неограниченные возможности для создания уникальных и оригинальных ароматов. Каждая комбинация спиртов имеет свои особенности, влияющие на стойкость, интенсивность и характер запаха.
Одним из наиболее популярных типов смешанных спиртов в парфюмерии является этиловый спирт с добавлением изопропилового спирта. Такая комбинация обеспечивает хорошую стойкость аромата и его равномерное распределение на коже.
Еще одной интересной комбинацией является смесь этилового спирта с глицерином. Глицерин значительно повышает увлажняющие свойства парфюмов и способствует их длительному сохранению на коже.
Некоторые парфюмеры также используют смешанные спирты, включающие в свой состав пропиленгликоль. Пропиленгликоль обладает свойством фиксации запаха, что делает аромат более стойким и продолжительным.
Каждый парфюмер имеет свои собственные предпочтения и часто создает свои собственные уникальные комбинации спиртов. Комбинирование различных спиртов позволяет создавать ароматы с разнообразными характеристиками, а также играть с их стойкостью и интенсивностью.
В парфюмерии смешанные спирты играют важную роль в создании уникальных ароматов. Они позволяют позволяют парфюмерам экспериментировать, находить новые сочетания, и заставляют нас влюбляться в запахи снова и снова.
Действие этанола на организм человека
В биохимии этанола существенную роль играет тот факт, что он образует растворы в широком диапазоне пропорций как с водой, так и с жирами. Является побочным продуктом метаболизма глюкозы, в крови здорового человека может содержаться до 0,01 % эндогенного этанола.
В зависимости от дозы, концентрации, пути попадания в организм и длительности воздействия этанол также может обладать наркотическим и токсическим действием. Под наркотическим действием обозначается его способность вызвать кому, ступор, нечувствительность к боли, угнетение функций ЦНС, алкогольное возбуждение, привыкание, а также его наркозное действие. Под действием этанола происходит выделение эндорфинов в прилежащем ядре (Nucleus accumbens), у страдающих алкоголизмом также в орбитофронтальной коре (поле 10). Тем не менее с юридической точки зрения этиловый спирт наркотиком не признан, так как это вещество не включено в международный список контролируемых веществ конвенции ООН 1988 года. В определённых дозах к массе тела и концентрациях приводит к острому отравлению и смерти (смертельная разовая доза — 4—12 граммов этанола на килограмм массы тела).
Основной метаболит этанола ацетальдегид является токсичным, мутагенным и канцерогенным веществом. Существуют доказательства канцерогенности ацетальдегида в экспериментах на животных; кроме того, ацетальдегид повреждает ДНК.
Длительное употребление этанола может вызвать такие заболевания, как цирроз печени, гастрит, некротизирующий панкреатит, язва желудка, рак груди, рак желудка и рак пищевода (то есть является канцерогеном), гемолитическая анемия, артериальная гипертензия, инсульт, стать причиной внезапной смерти людей, страдающих ишемической болезнью сердца; может вызвать серьёзные нарушения обмена веществ. Алкоголь может увеличить риск рождения ребёнка с врождёнными аномалиями нервной системы и обусловить задержку роста.
Употребление этанола может вызвать оксидативное повреждение нейронов головного мозга, а также их гибель вследствие повреждения гемато-энцефалического барьера.
Злоупотребление алкогольными напитками может привести к клинической депрессии и алкоголизму.
Приём алкогольных напитков на фоне приёма лекарств очень нежелателен, так как алкоголь извращает действие лекарственных средств и вследствие этого становится опасен для жизни человека. Отрицательное влияние алкогольных напитков на результаты фармакотерапии многообразно и зависит от различных факторов: индивидуальных свойств больного, его чувствительности, тяжести заболевания, но во всех случаях у пациентов, принимающих лекарства и потребляющих алкоголь, эффективность фармакотерапии ослабляется, а порой и сводится на нет.
Этанол может в небольших количествах синтезироваться в просвете желудочно-кишечного тракта в результате процессов ферментации углеводной пищи микроорганизмами (условный эндогенный алкоголь). Существование биохимических реакций с синтезом этанола в тканях организма человека (истинно эндогенный алкоголь) полагается возможным, но не доказано к настоящему моменту. Количество эндогенного алкоголя редко превышает 0,18 промилле, что находится на границе чувствительности самых современных приборов. Обычный алкотестер такие количества определить не может.
Опасность вдыхания паров
Этанол может наносить вред здоровью и при вдыхании паров при достаточно большой концентрации. В РФ установлена ПДК этого вещества: 1000 мг/м3 (среднесменная, за 8 часов) и 2000 мг/м3 (максимально-разовая), 4 класс опасности.






























